近日,工学院生物医学工程系董康立博士以第一作者,在Nature Portfolio旗下期刊Communications Biology(中国科学院一区)发表题为“Optimal stochastic tracking control for brain network dynamics”的研究论文。该研究以脑卒中及卒中后失语等神经功能障碍康复中的脑刺激参数优化问题为例,将网络控制理论从“将大脑推到某个目标状态”的经典框架,拓展为“让病理脑网络动态持续跟踪健康目标动态”的最优随机跟踪控制框架,为个体化、低能耗脑刺激干预提供了新的计算思路。
脑网络控制理论(Network Control Theory, NCT)近年来被广泛用于解释脑刺激效应,并探索经颅磁刺激(TMS)、经颅直流电刺激(tDCS)等非侵入式脑刺激技术的优化范式。传统最优脑网络控制研究通常将目标设定为:在某一时间点把大脑从一个状态转移到另一个目标状态。然而,大脑活动本质上是连续演化的时间序列,同时还包含自发神经波动和随机噪声;用“状态”描述病理脑动力学,难以全面刻画真实脑刺激干预的目标。
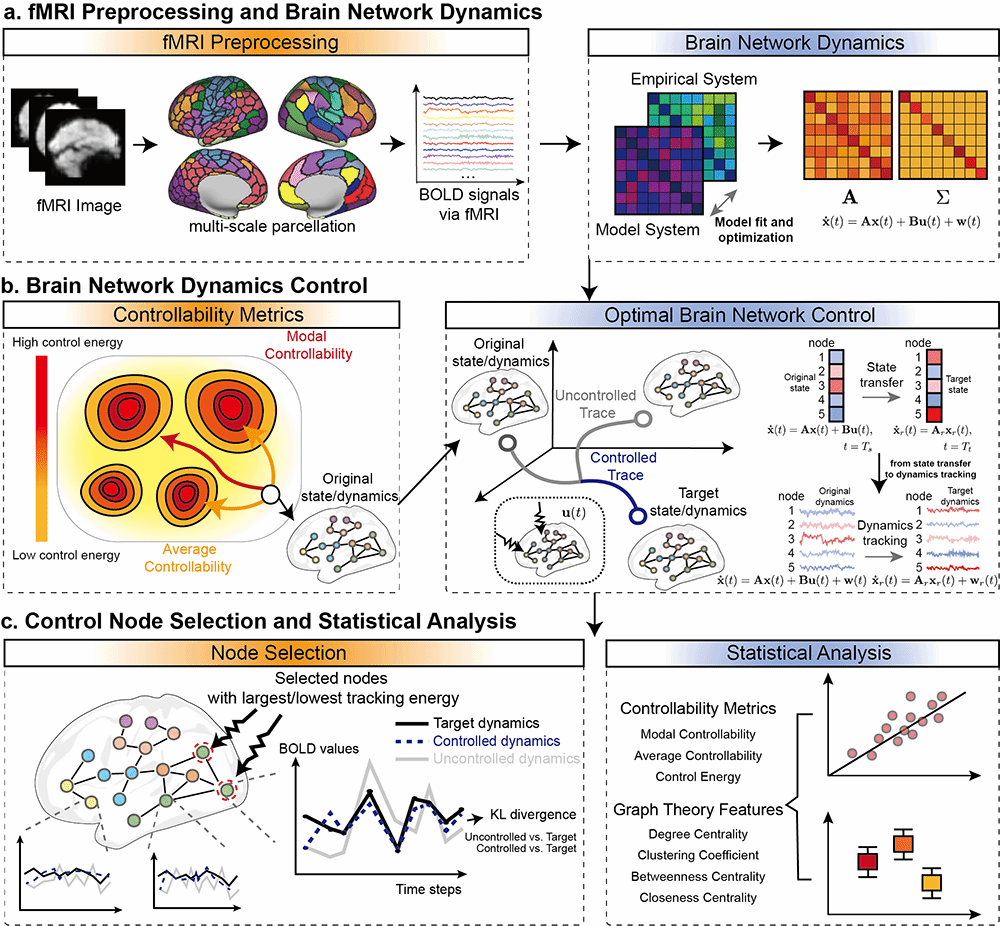
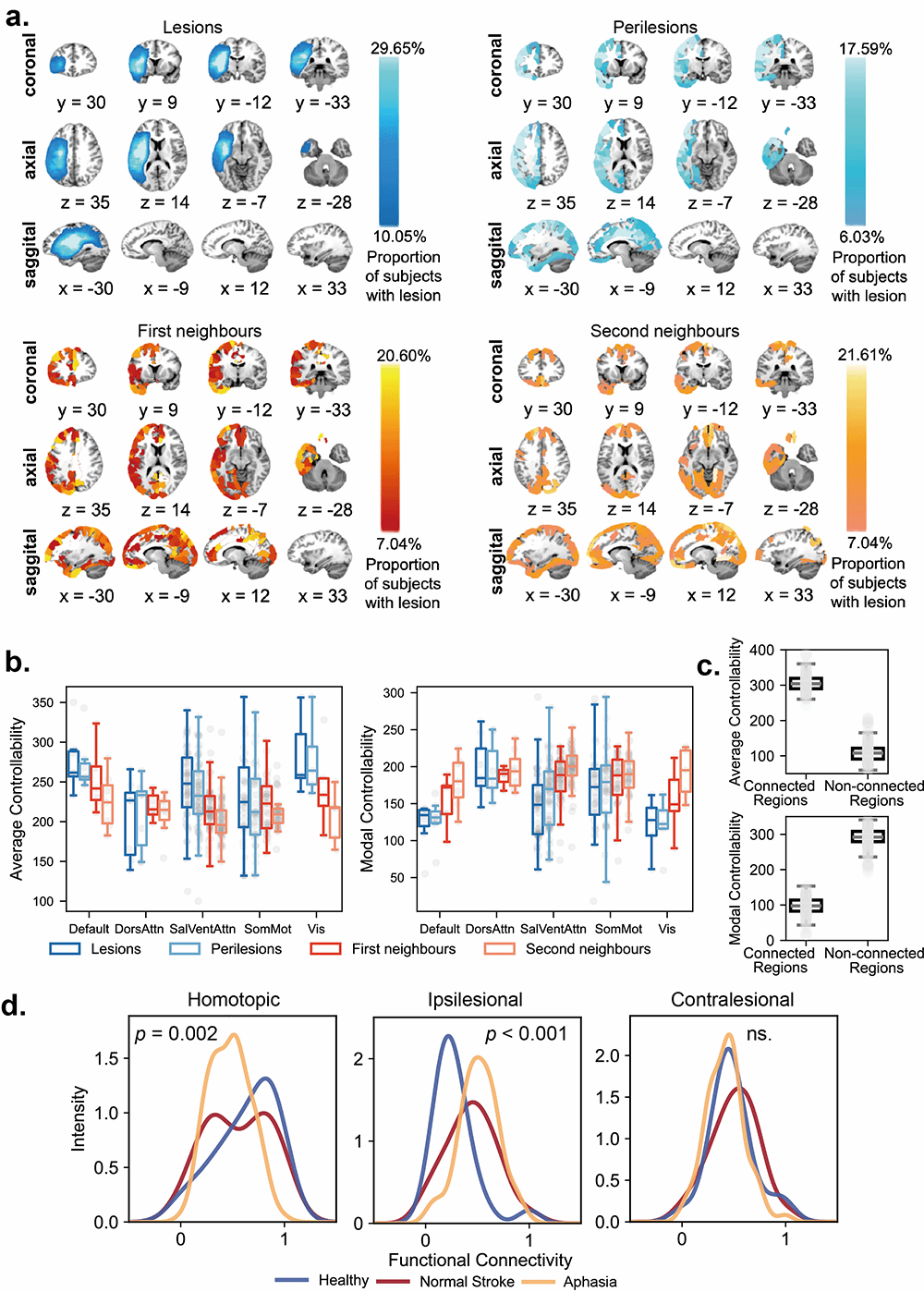
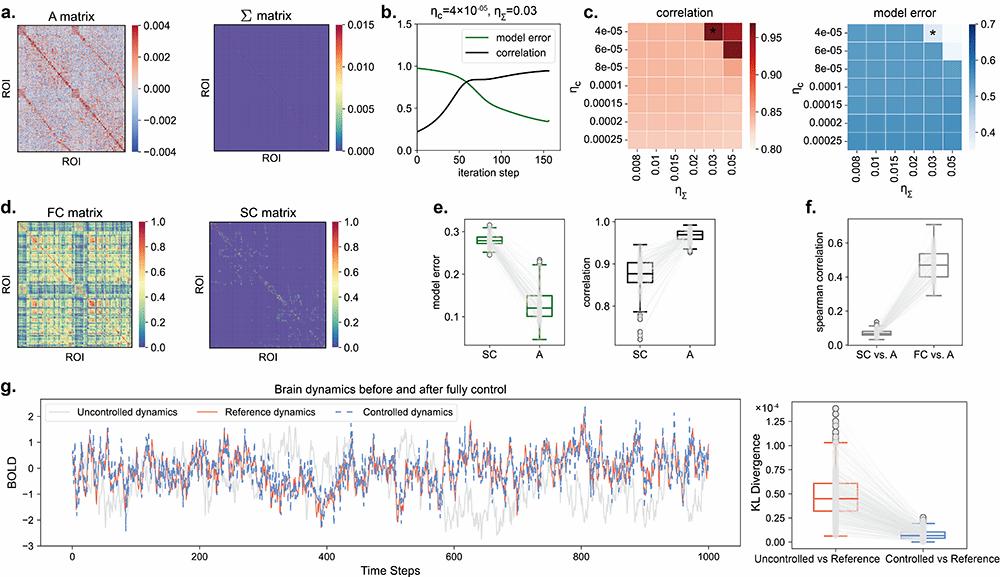
针对这一问题,本研究提出最优随机跟踪控制框架,将控制目标从“到达单一目标状态”拓展为“使病理脑网络动力学与健康目标动力学在统计特征上保持同步”。研究以脑卒中及卒中后失语患者为例,基于功能磁共振成像(fMRI)和弥散加权成像(DWI)数据,利用梯度下降方法估计脑网络动态系统中的耦合矩阵和方差矩阵,并在此基础上计算不同控制节点的跟踪能量和控制效果。
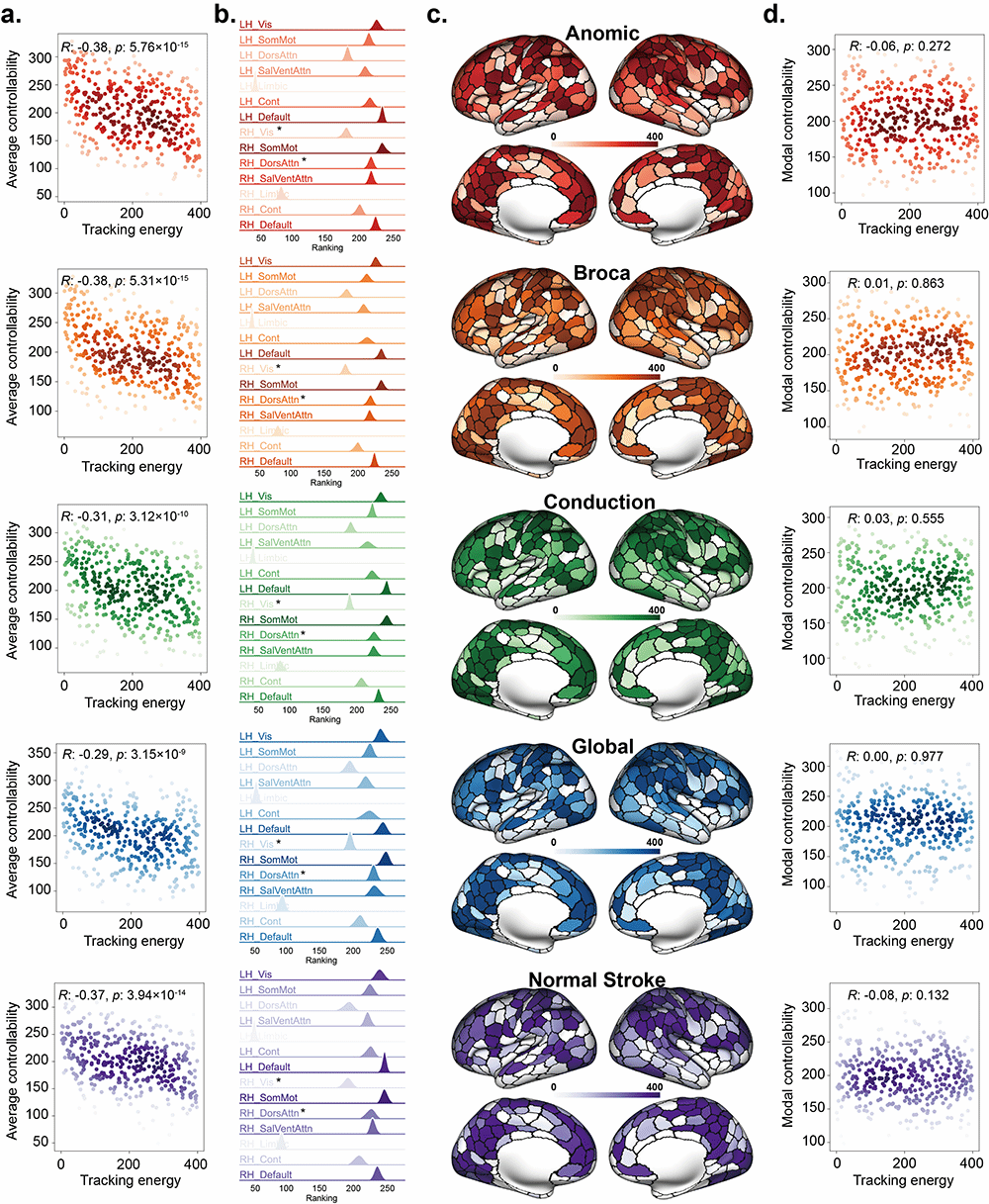
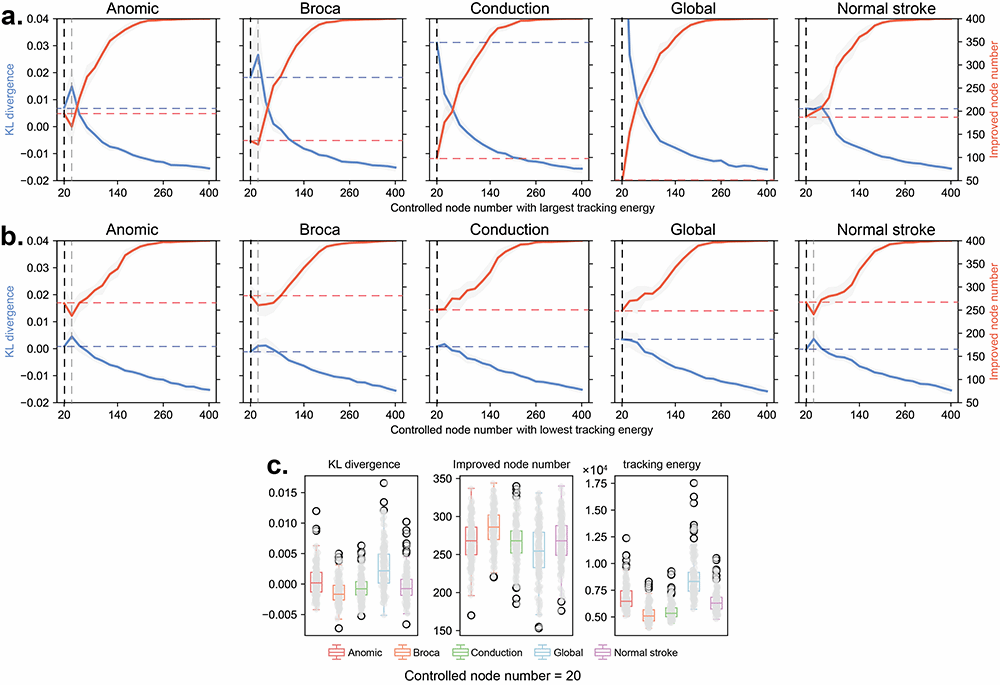
结果表明,随机跟踪控制能量与脑网络平均可控性呈显著负相关,而传统最优状态转移控制的能量更大程度依赖于所选目标状态本身。在100维脑网络系统中,仅控制5个跟踪能量最低的节点,即可改善超过90%节点的动力学表现。该发现提示,最优随机跟踪控制有望为卒中、卒中后失语等神经系统疾病的脑刺激干预提供低成本、个体化的理论指导。
本研究将脑网络控制从“最优状态转移”推进到“最优动力学跟踪”。这一转变使模型能够同时考虑脑活动的连续时间演化和随机波动,更符合脑刺激干预希望长期改善病理脑动态的实际目标。研究结果表明,最优随机跟踪控制能量与平均可控性之间存在稳定关系,可用于识别更低成本、更具效率的潜在刺激节点。
在临床应用层面,该框架为需要神经调控干预的脑疾病提供了新的计算工具:一方面,它可以评估不同脑区作为刺激靶点时的理论动力学控制成本;另一方面,它能够帮助探索“最少控制节点实现最大动态改善”的刺激策略。未来,结合脑动力学模型、语言相关皮层区域分析以及多模态神经影像数据,该方法有望进一步服务于精准脑刺激和个体化神经康复。
来源:工学院


 网站地图
网站地图