重庆大学冯璋/汕头大学倪绍飞/四川轻化工大学杨义团队报道了一种由双(三甲基硅基)氨基钠和联硼酸频哪醇酯参与下的羰基衍生物的可控去饱和二硼化反应,能够快速从易得的环己酮衍生物合成1,3-芳基二硼酸酯。该转化无需金属催化剂和添加剂,条件温和,官能团耐受性好,可实现多种药物相关分子的后期二硼化。
芳基硼酸酯能够构建多样化的C-C键和C-X键,是有机合成中不可或缺的分子。目前开发的构建芳基C-B键的方法主要以芳烃、芳基卤代物或酚类衍生物作为起始底物,非芳香底物尤其是羰基化合物直接转化为芳基硼酸酯的反应还未被充分探索。更重要的是,现有的方法大都聚焦于单硼化反应,芳基二硼酸酯的高效且高度区域选择性的转化具有很大的挑战。芳基二硼酸酯是合成和材料科学中宝贵的中间体,传统方法通常依赖于过渡金属催化的C-X键的硼化,或芳基金属试剂与硼亲电试剂的反应。铑和铱催化的C–H二硼化也有报道,但控制区域选择性仍具挑战性。大多数现有方法仍依赖对空气和湿度敏感的有机金属试剂,或者昂贵的催化剂和配体,使得其实际应用变得复杂。
因此,作者提出了一种顺序的硼化芳香化策略,直接从易得的环己酮衍生物合成1,3-芳基二硼酸酯。作者设想,合适的碱可以同时通过阴离子-二硼相互作用激活二硼试剂,并通过金属阳离子配位到羰基氧来促进烯烃的C–O键活化。这种双重活化将使烯烃C–O键的原位硼化成为可能,随后进行烯丙位C–H硼化,最终通过芳香化推动去饱和过程,生成芳基二硼酸酯。然而,实现这一策略存在几个根本性挑战:(1)在无过渡金属催化的情况下实现惰性烯烃C–O键和烯丙位C–H键的硼化;(2)对区域选择性二硼化实现精确控制;(3)在使用强还原性二硼试剂的体系内实现氧化性去饱和化(图1)。
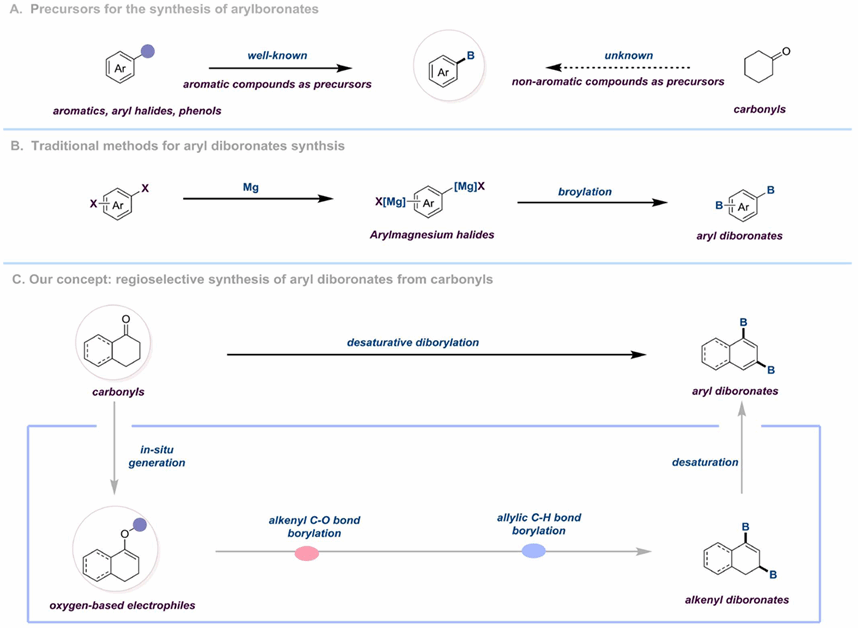
图1. 对羰基进行可控去饱和硼化以获取芳基二硼酸酯
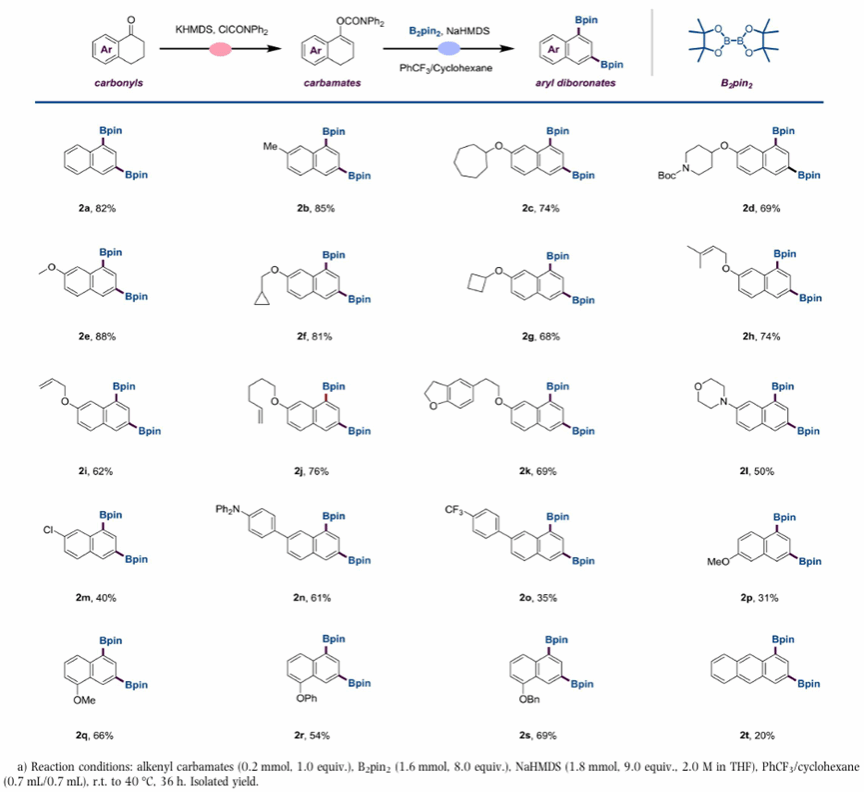
确定最佳反应条件后,作者评估了NaHMDS促进的去饱和二硼化反应的底物范围(表2)。该反应表现出优异的官能基耐受性,能够容纳烯烃、烯丙基、胺基、OPh、OBn、氯和三氟甲基等。值得注意的是,该体系能容忍烷基链上的应变环如环丙烷和环丁烷,并且对内部和端位烯烃基团都保持高效率,后者通常在过渡金属催化的硼化反应中较为敏感。
表2. 底物范围的考察
通过生物活性分子的后期二硼化转化,进一步证明了该方案的合成价值(图2)。由油醇、香茅醇和法尼醇衍生的底物表现出优异的反应性,其内部烯烃基团在反应条件下保持完整,能以良好产率获得所需的芳基二硼酸酯。尽管放大到克级实验后效率有所下降,但仍能以合成有用的产率获得所需的芳基二硼酸酯。此外进行了一锅法尝试,能够以中等产率快速将羰基前体直接转化为芳基二硼酸酯,无需中间纯化。
芳基二硼酸酯2a可以高效转化为芳基二氯化物、芳基二溴化物和芳基二碘化物。此外,芳基二硼酸酯在钯催化下容易发生铃木偶联反应,高效产生1,3位官能化萘衍生物。值得注意的是,1位的硼基表现出比3位更高的反应性,因而能够对芳基二硼酸酯进行连续的差异化修饰,为1,3位官能化萘衍生物的合成提供了一种可用的方案。
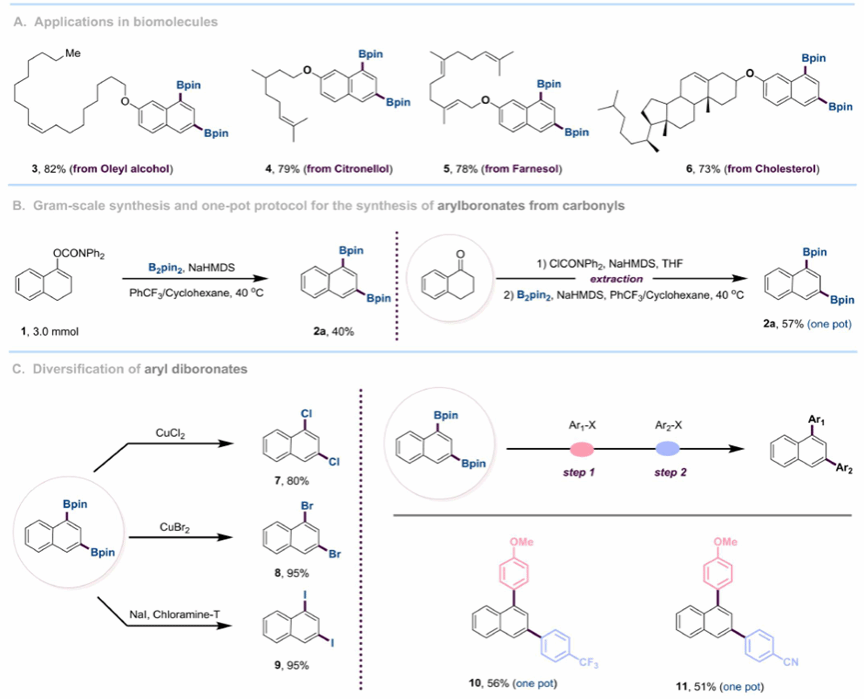
图2. 产物的衍生化及应用
作者进一步研究了二硼化反应机制(图3)。芳基单硼酸酯3a′在标准二硼化条件下无法转化为芳基二硼酸酯2a。此外,该体系中能够分离得到烯烃单硼酸酯4a。然而,4a并未经历第二次硼化形成芳基二硼酸酯2a,相反,它仅以适中的产率产出芳基单硼酸酯3a′。这些观察表明烯基单硼酸酯4a并非二硼化途径中的中间体。令人欣慰的是,作者通过HRMS成功检测到高度反应性的烯基二硼酸酯4b,表明其在二硼化反应中具有关键中间体的潜力。为了进一步理解前所未有的去饱和过程,作者进行了对照实验。这些实验表明,在脱气条件下反应顺利进行,且在没有二硼试剂的情况下不会发生脱饱和。这些结果强烈表明,促成去饱和步骤的是二硼试剂而非氧气。
基于这些发现,作者提出了这些硼化反应的合理机制。在二硼化反应中,烯基氨基甲酸酯1首先发生烯丙位C–H键硼化,产生了单硼化产物5b。随后,第二次对烯烃C–O键进行硼化,生成了烯基二硼酸酯4b,随后进行去质子化和去饱和处理,以获得所需的芳基二硼酸酯2a。另外,为更好地理解去饱和硼化过程,作者还采用了DFT计算来探讨反应机制。
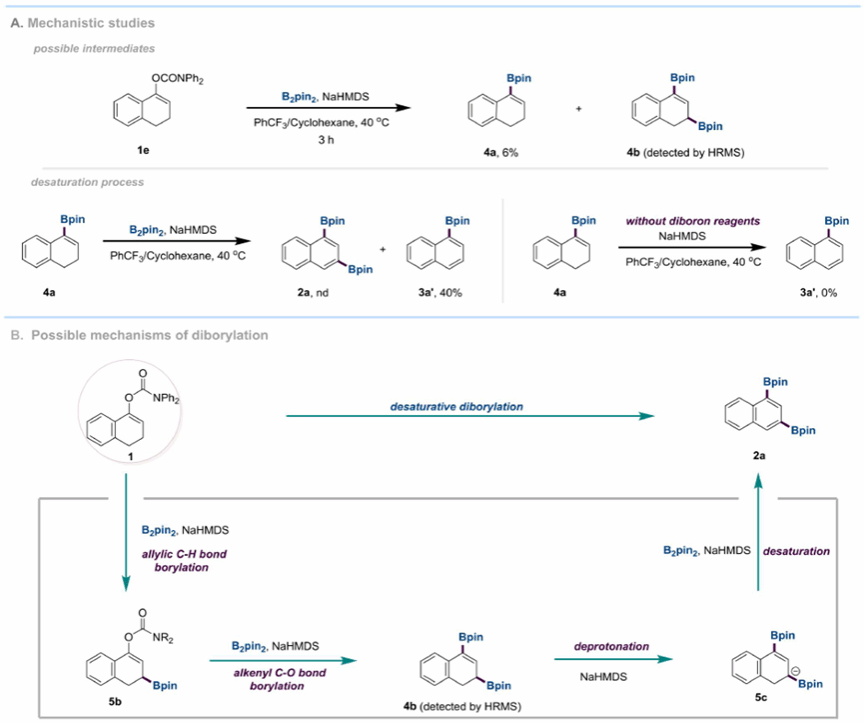
图3. 机理研究
综上所述,作者开发了一种由NaHMDS促进的无过渡金属和添加剂的策略,用于直接从羰基化合物合成芳基二硼酸酯。该方法官能团耐受性好,适合生物活性羰基衍生物的后期官能化。实验和计算研究的综合揭示了NaHMDS和二硼试剂在推动去饱和过程中的关键作用。这项工作开辟了非芳香前体转化为芳基二硼酸酯的新路径,并揭示了碱/二硼试剂系统全新的反应性,这可能激发新的去饱和化转化的发展。
相关成果近期发表于Science China Chemistry,详细内容见:Shi C#, Ma C#, An X#, Sun M#, Geng S, He Y, Yang Y*, Ni S*, Feng Z*. Controlled desaturative diborylation of carbonyls. Sci China Chem, 2026, DOI: 10.1007/s11426-025-3345-5.